据《ABC新闻》10月15日报导,由再生元制药(Regeneron Pharmaceuticals)研究而成的埃博拉治疗药物Inmazeb,已在周三获得美国食品药品监督管理局(FDA)的批准。所有埃博拉患者将面临六至九成的死亡率,而根据研究,经过注射Inmazeb后,约2/3的患者将会康复。

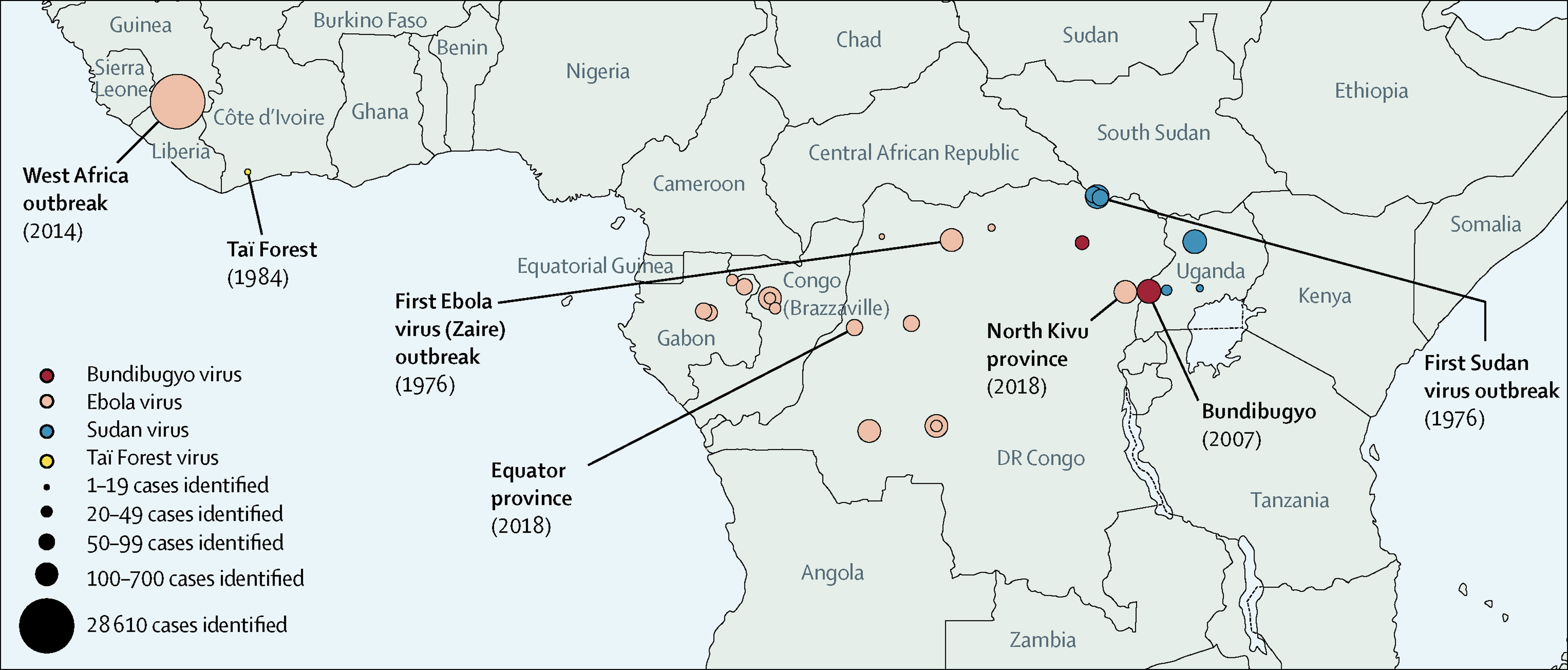
据悉,刚果(Congo)在2018年爆发了一场大规模的埃博拉疫情,死亡人数高达2.3千人。当时,共有4款包括Inmazeb在内的埃博拉治疗药物在这场疫情中被进行临床试验。研究显示,使用Inmazeb和第二款治疗药物的患者明显有较高的存活率。
埃博拉病毒专家,利亚·利普希克(Leah Lipsich)在接受访问时表示,Inmazeb中含有三种抵抗埃博拉病毒的抗体,因此埃博拉病毒很难将所有抗体消灭并对其免疫。报导称,共有681名埃博拉患者被注射四种治疗药物中的其中一种。在4星期后,约2/3使用Inmazeb和第二款治疗药物的患者存活了下来,而使用另外两款药物,ZMapp或remdesivir的患者则只存活了一半。
据悉,获FDA批准是所有美国药品制造商将药品投放到市场的第一步,即使患者通常来自热带或发展中国家。FDA的药品准证将会使再生元制药把药物带到非洲的过程更为快速并顺利,但获得批准的过程将会是繁琐并漫长的。
根据研究,埃博拉病的的传染力非常强,并主要通过身体和体液接触传播,症状包括发烧、肌肉酸痛、呕吐、肾脏和肝脏损伤与内、外出血。美国政府向再生元制药的埃博拉病毒药物研究计划投入了非常多的资金,并预计将在未来六年内向再生元制药购买上千剂Inmazeb当作战略国家储备(Strategic National Stockpile)。埃博拉病毒虽然在美国并不常见,但仍然会在从埃博拉疫情区返回的人员身上发现埃博拉病毒。报导称,Inmazeb的研究期被缩短以确保Inmazeb能够尽早投入市场。


