据路透报道,最新公布的法庭文件和其他记录显示,默克公司和美国监管机构,在2011年更新一种受欢迎药物的标签时,决定不警告消费者潜在的风险,他们知道服用默克公司抗脱发药物保法止(Propecia)的男性,有自杀行为的报告。
默克公司的内部记录在1月底被公开,当时纽约布鲁克林的一名联邦法官批准了路透社2019年的一项动议,以公开在数年诉讼中提交的11份文件,这些文件指控,药物保法止导致持续性性功能障碍和其他有害副作用。
自2011年做出警告决定以来,美国食品与药品监督局(FDA)已经收到了700多份关于服用保法止或非专利药的人自杀和有自杀想法的报告,至少100人死亡。
在此之前,在此药物上市的头14年里,FDA收到了34份此类报告,其中包括10例死亡。
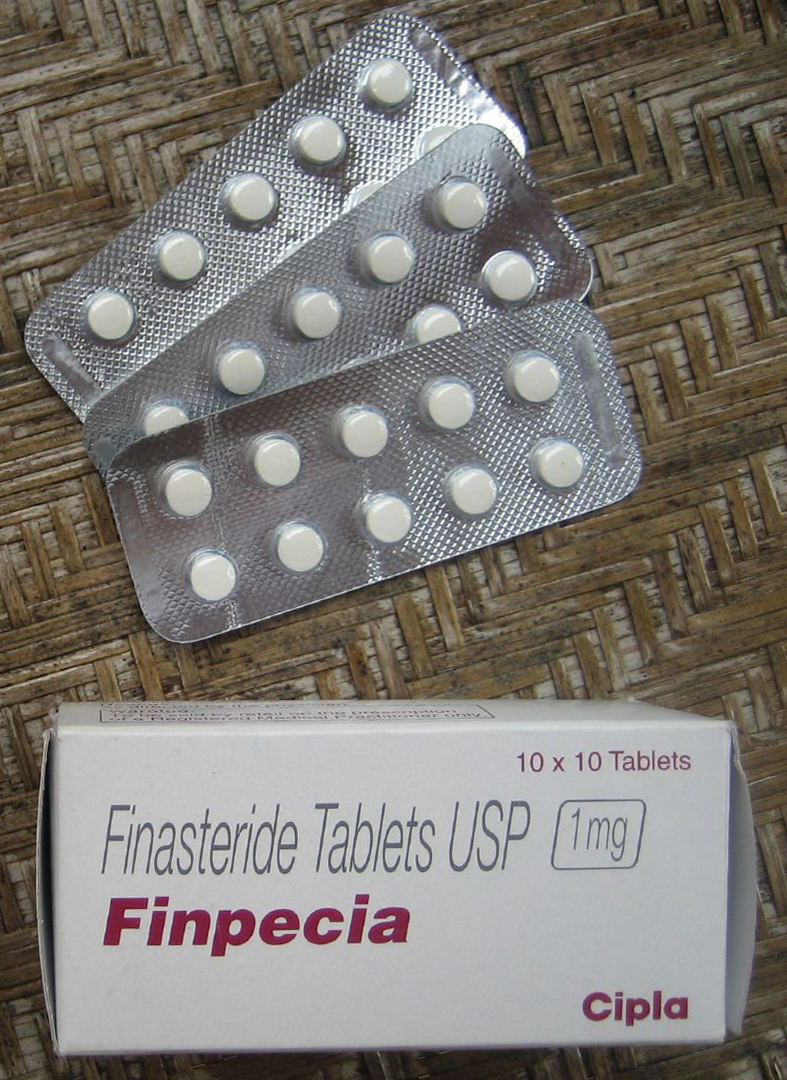
健康数据公司IQVIA的数据显示,2020年,保法止的主要成份,非那雄胺(Finasteride)在美国每年用于治疗脱发的处方增加到240万份以上,是2015年的两倍多。
欧洲和加拿大的监管机构以服用非那雄胺的男性中出现类似报告为由,要求在标签上注明自杀念头的警告,不过他们指出,研究并没有证明这种药物会导致这种念头。时至今日,美国的标签上没有提及自杀或自杀念头。
早在2009年,默克公司就知道200多份关于服用保法止的男性出现抑郁症状的报告,包括自杀念头,这是根据该年的内部“风险管理”评估得出的。该公司认为,关于严重抑郁症和自杀行为的报告太少,这些案例的细节也不够多,需要对安全数据进行“常规”监控。
2011年,也就是默克分析风险两年后,美国FDA正在考虑默克公司提出的,将“抑郁”作为潜在风险添加到药物标签的要求,而没有给出与自杀有关的警告。根据此前未报道的政府文件,FDA分析师不同意添加与自杀有关的警告。但监管机构最终同意了默克的要求,理由是自杀人数低于人们对这一组患者的预期。

一些医学研究人员和患者权益倡导人士说,默克公司和FDA让美国消费者对非那雄胺潜在的生命危险一无所知。
“不应该让任何家庭在事后知道这件事,”金姆·维特查克说,她是美国食品和药物管理局精神病药物顾问团的消费者权益倡导者。
2003年,她的丈夫在服用抗抑郁药治疗失眠五周后自杀身亡,她呼吁制药公司和监管机构对此发出更强烈的警告。默克“本来有机会在标签上写上自杀,但他们不想这么做,因为这事关销量。”
内分泌学家、哈佛医学院教师迈克尔·欧维格表示,他自己的研究发现了非那雄胺和自杀行为之间的可能联系,他说默克公司对风险分析的处理和FDA对公众隐瞒关键信息的不作为。欧维格说,默克公司“肯定应该提供一个更完整的画面。”
默克公司在给路透社的一份声明中说,“科学证据并不支持保法止和自杀或自杀意念之间的因果关系,这些术语不应该包括在该药物的标签中……默克公司不断与监管机构合作,以确保对潜在的安全信号进行仔细分析,并在适当的情况下,将其包含在保法止的标签中。”
默克公司在过去的声明中说,自20世纪90年代末以来,保法止已经安全地给数百万男性进行治疗。它还在法庭上提出,“过早脱发本身,即使用保法止的情况,与自卑、身体形象差和抑郁有关。”
FDA在一份声明中表示,它“继续监测保法止上市后的安全数据。”
总而言之,FDA指出,FDA数据库中出现的报告“并不意味着该药物导致了不良事件”,医疗问题可能源于“正在治疗的潜在疾病,同时服用其他药物引起的疾病,或因其他原因发生的疾病。”
FDA拒绝进一步评论其对保法止的处理以及有关自杀的报道。
默克公司对潜在自杀风险的分析在法庭上保密了三年多,直到路透社介入后才公之于众。最近公开的文件中的见解与路透社2019年“隐藏的不公正”调查的结果相呼应,该调查揭示了美国法官通常允许消费品制造商在诉讼中,以保密的方式提交与公共健康和安全相关的信息。
他们经常在没有解释的情况下这样做,尽管在其他大多数司法管辖区,他们被要求提供解释。
路透社的调查发现,近几十年来,成千上万的美国人因涉嫌存在缺陷的产品(包括药品、汽车和医疗设备)而死亡或严重受伤,而本可以提醒消费者和监管机构注意潜在危险的证据仍未找到。
在批准路透公开默克文件的动议时,美国地方法官Peggy Kuo上月裁定,默克继续保密的理由”太弱,无法克服普通法下对获取默克文件的较低推定。”
除了风险管理计划,Peggy Kuo还公开了默克公司的其他文件,包括该药物上市前的一份内部营销报告,以及与监管机构就性功能障碍的一些沟通。路透社从FDA维护的一个单独的在线资源库中,获得了有关自杀的文件。
2010年,在审查默克公司的提案时,在保法止的标签上增加了潜在的抑郁风险,FDA的安全评估人员也建议增加自杀想法和自杀行为的警告,他们注意到9名服用非那雄胺的患者,有自杀和其他自杀行为的报告,路透社查阅的FDA文件显示。
默克公司和政府监管机构分析的自杀行为报告,被称为“不良事件”报告,由消费者、医生和其他公众提交。它们由美国监管机构和其他国家的药品安全机构汇编在一个公共数据库中。
FDA安全评估员Namita Kothary在她2010年11月的报告中写道,由于信息不完整,这九起自杀事件难以评估,“然而,我们不能排除非那雄胺可能对这些事件有一定的影响。”
另外两名FDA审查员不同意。这两位医生,艾米·沃伊塔克和大卫·凯特尔表示,数据支持将抑郁症添加到标签中。然而,根据他们2010年12月的报告,自杀倾向应该被删除,因为自杀意念、企图和死亡的数量“低于这一患者群体的预期”。
欧洲药品管理局发现非那雄胺和抑郁症之间的关系难以评估,但仍然需要在2017年对自杀倾向应该被删除发出警告,根据会议记录,部分原因是保法止不是用于严重病情的处方药。医生和病人对一种治疗危及生命的健康问题的用药,和不那么严重的问题用药的风险衡量通常是不同的。
当加拿大卫生部要求其在2019年发出警告时,它注意到截至2018年9月,国际上有368份关于接受非那雄胺治疗的患者自杀事件的报告。默克公司没有回应有关这些监管举措的问题。
1997年,FDA批准了保法止的上市,其销售额在21世纪头十年稳步攀升,2010年达到4.47亿美元的峰值。不久之后,默克的专利到期了。非那雄胺的总体销售仍然强劲,因为较便宜的仿制药已经进入市场。
有关潜在自杀风险的新信息出现,是由于长期以来对药物相关的性问题存在争议。
默克公司的标签从一开始就说,保法止导致近4%的临床研究参与者出现性功能障碍。然而,2009年的风险管理报告也显示,该公司意识到一些男性在停止服用该药物后,性功能障碍问题继续存在。

FDA在2012年批准了默克公司的要求,增加了对停药后继续存在的勃起功能障碍以及“性欲障碍、射精障碍和性高潮障碍”的警告。即便如此,默克公司当时仍表示,科学证据并不能确定保法止会导致持续性的性功能障碍。
这一警告引发了1100多起针对默克的诉讼,这些男性声称他们的性问题,在停止使用保法止后仍持续了很长时间。2018年,默克同意以430万美元的总价了结了大部分诉讼。
路透社在2019年报道称,在和解之前,原告律师声称,默克在修改该药的原始标签时,低估了在临床试验中出现性症状的男性人数,以及这些症状持续的时间。
上个月公布的2009年风险管理报告显示,虽然抑郁症在临床试验中没有作为风险出现,但默克公司在1998年至2008年收到218份全球抑郁症报告后,认为这是一个 “重要的潜在风险”。其中,10例涉及严重抑郁症,另外9例涉及自杀行为。
默克公司指出,抑郁症报告和涉及自杀行为的9份报告都存在局限性。四人提供的信息“不足以进行全面评估”。其中3名男子有其他病症,对2名男子来说,症状是在他们停止服用药物后出现的。
“一份致命报告来自警长办公室,描述了一名男子开枪自杀,”报告称。“法医认为这起事件与保法止无关,此外,报告提供的信息不足,无法进行评估。”
默克在给路透社的声明中表示,不良事件报告只反映了提交报告人的意见。该公司表示,“虽然鼓励消费者和医疗保健专业人员报告不良事件,但这种反应可能与正在治疗的潜在疾病有关,或由同时服用的其他药物引起,或因其他原因发生。”
乔治亚医学院精神病学和健康行为系主任沃恩·麦考博士同意,依赖不良事件报告来监测药物安全有其局限性。然而,他说,这些限制之一是,伤亡往往被低估,因为人们不熟悉过程或没有时间审查一个具体的案例。
他说,对于保法止和自杀想法之间的潜在联系,有一种看似合理的生物学解释。这种药物会降低一种睾丸激素相关的激素,而这种激素反过来又会影响体内产生的抗抑郁类固醇。
“我们有理由怀疑,”麦考博士称。


