据《纽约时报》报道,周三(12月30日)英国成为第一个紧急批准阿斯利康(AstraZeneca)和牛津大学(University of Oxford)共同研发的新冠疫苗的国家,为一种廉价、易于储存的疫苗开辟了道路,未来世界上很多人将依赖这种疫苗来帮助结束大流行。
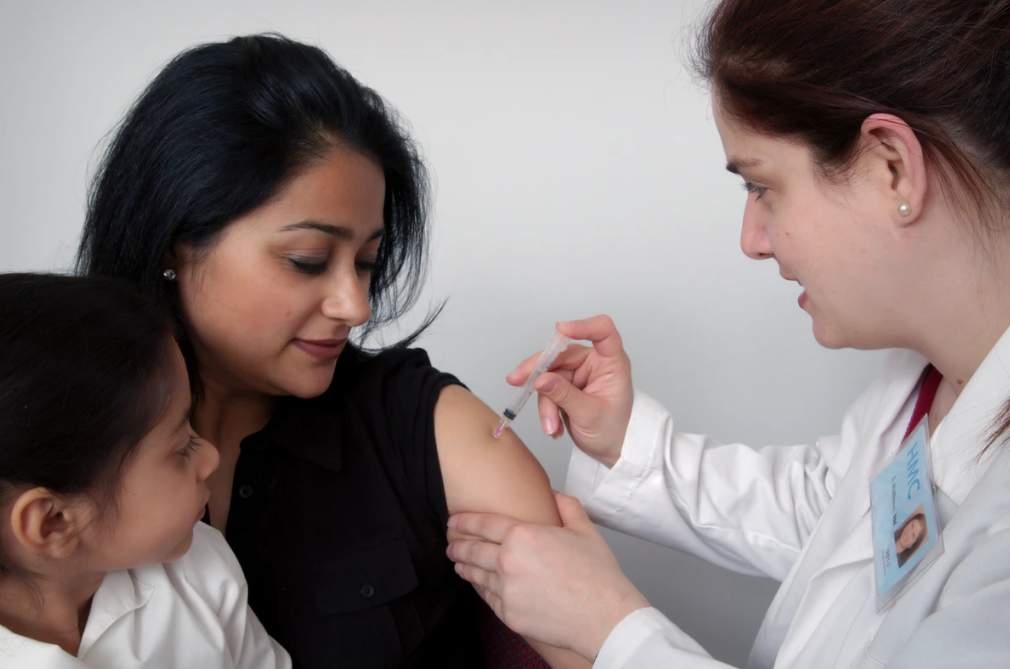
英国的医院已经被一种新的、传染性更强的变种新冠病毒所攻占,该决定提供了一些缓解疫情的希望。卫生服务部门准备很快每周在足球场和赛马场的临时地点为100万人接种疫苗。
牛津-阿斯利康联合注射将成为世界上最主要的疫苗接种方式。每剂疫苗3至4美元(约合人民币20-26元),只是其他一些疫苗成本的一小部分。它可以在正常的冷藏温度下运输和储存6个月,而不是像辉瑞和莫德纳的疫苗所要求的那样放在超冷的冷冻箱内,这使得它更容易用于世界上较贫穷和偏远地区的人们。
阿斯利康公司的疫苗在临床试验中显示了62%的效力,比辉瑞公司和莫德纳的疫苗大约95%的效力要低很多。不过,阿斯利康的疫苗在一组较小的志愿者中显示出90%的疗效,这些志愿者只接受了半强度的初始剂量。
除了剂量问题,英国的卫生服务还必须弄清楚如何说服人们接种这种功效较低的疫苗,但尽管如此,可能会加快结束这场疫情。该授权依据的是英国和巴西的三期临床试验数据。印度的药品监管机构预计也将很快决定是否批准这种疫苗,它正在由当地的疫苗生产商血清研究所生产。
在美国,这一决定还远未做出,美国食品和药物管理局(FDA)正在等待另一项临床试验的数据。由于监管机构调查英国一名参与者的一种疾病是否与疫苗有关,该研究于9月份暂停,并推迟了近7周——比其他国家要长得多。美国监管机构最终允许审判继续进行。
最近几天,研发出这种疫苗的牛津大学科学家们在大西洋两岸展开了一场辩论,讨论是否要推迟计划中的第二剂这种疫苗和其他疫苗,以便让更多的人获得单剂疫苗的部分保护。牛津疫苗计划负责人安德鲁·波拉德在接受电台采访时表示,推迟第二剂疫苗的接种,“让尽可能多的人开始接种是很有意义的”。
阿斯利康公司设定了比其他疫苗生产商更雄心勃勃的生产目标,称其2021年有望生产多达30亿剂疫苗。如果按照每人接种两剂的标准,就足以让全世界近五分之一的人接种。该公司承诺,至少到2021年7月,该产品将在全球以成本价销售,并在较贫穷的国家并在贫困国家永久提供。
但该公司也一直被沟通失误所困扰,这些失误破坏了其与美国监管机构的关系,并引发了人们对该疫苗能否经受住公众和科学的严密审查的怀疑。这些失误使得该疫苗在美国的上市时间推迟,美国食品和药物管理局的重要官员震惊地得知,九月份暂停临床试验的消息不是来自阿斯利康,而是来自新闻媒体。
这些挫折并没有挫伤英国人对该国领先的国产疫苗的热情,分析人士说,如果这种疫苗迅速推出,可能会让在首相约翰逊的任期内走上正确的道路。
英国订购了1亿剂疫苗,其中4000万剂预计到3月份即可供应,这使阿斯利康疫苗接种战略处于关键地位。自从12月2日批准辉瑞公司的疫苗以来,英国已经用它为成千上万的人接种了疫苗。但该国一直在医院和医生办公室以外的地方努力管理它,这使得一些最优先的接受者,比如疗养院的居民,仍然处于劣势。
在英国参加临床试验的一小部分志愿者由于测量问题,第一次接受了半剂量的剂量。牛津大学聘请了一家外部制造商为试验生产疫苗。但是当研究人员收到疫苗样本时,他们发现它的强度是制造商使用不同测量技术时发现的两倍。由于不知道该相信哪种测量方法,研究人员决定将剂量减半,以确保志愿者不会得到原定剂量的两倍。后来,牛津大学的研究人员证实他们的读数太高了,于是他们在第二次注射时回到了原来的计划剂量。
在较小的一组2741人中,他们接受了一半剂量的第一剂疫苗或脑膜炎球菌疫苗作为对照,疫苗的有效性被发现为90%。然而,这些参与者都没有超过55岁,因此很难知道这些结果是否适用于老年人。

阿斯利康和牛津大学的科学家表示,他们不知道为什么半剂量的初始剂量如此有效。但他们对自己的结果表示有信心,特别是发现在临床试验中没有人接种疫苗后再感染住院。
阿斯利康首席执行官帕斯卡尔·索里奥特在采访中告诉《伦敦时报》:“我们认为我们已经找到了制胜的配方,以及如何获得两剂药后的疗效。但我不能告诉你更多,因为我们会在某个时候发表。”该公司还没有公布任何证据表明其疗效能达到辉瑞或Moderna的水平。
牛津大学的科学家们本月早些时候在《柳叶刀》上发表了临床试验的中期发现。这些试验即将得到的最终结果预计不会与中期数据有显著不同,这在临床研究中很常见。
截至上周,阿斯利康在美国的试验已招募了超过27,000名参与者,略低于其30,000人的目标。“曲速行动”负责人蒙塞夫·斯拉维在上周的新闻发布会上表示,试验可能会有结果,如果结果积极,美国将在2月或3月获得紧急授权。
阿斯利康公司的高管已经公开提出了收集更有前途的给药方案的额外数据的几个想法。他们于11月的时候说,他们正在考虑在正在进行的美国试验中增加助力,或启动一个新的全球试验。但到目前为止,这些想法都没有实现。


