巴伦报道说,最近几周,投资者对新型肥胖症药物的狂热开始转移了焦点,从已经上市的注射剂转向了未来几年可能上市的药片。
虽然对注射用蒙扎罗(Mounjaro)的热情,已经让礼来公司成为全球最有价值的制药公司,市值超过 4250 亿美元,但会长期影响蒙扎罗及同类产品的,可能是口服减肥药物。
最近几天,一些公司在重要的医学会议上提交了新的数据,减肥药领域的情况已经有所明朗。礼来公司和诺和诺德公司(Novo Nordisk)是这一领域的领军企业,辉瑞公司和硕迪生物(Structure Therapeutics)也有望在这一领域抢到一席之地。
人们希望肥胖药片能提供新型注射剂的大部分疗效,却不会有生人起鸡皮疙瘩的针头,而且价格更低。每天注射是一个令人倒胃口的事情,而保险公司也不太可能愿意无限期地为昂贵的注射剂买单。
药片可能是一种解决方案。药片成本更低,服用更方便,患者可以长期服用,从而大大拓展了潜在市场。药片也比注射剂更容易制造,可以缓解供应紧张的问题。
杰富瑞医疗保健策略师威尔·塞武什写道:”这类药物没有下行通道,医生们已经承认这是肥胖症慢性治疗类别。口服维持疗法打开了肥胖症市场,缓解了支付方对定价的担忧,而且可能不会稀释利润率。”
问题依然很多,但投资者正在密切关注。以下是值得跟踪的药物。
诺和诺德的High-Dose Semaglutide
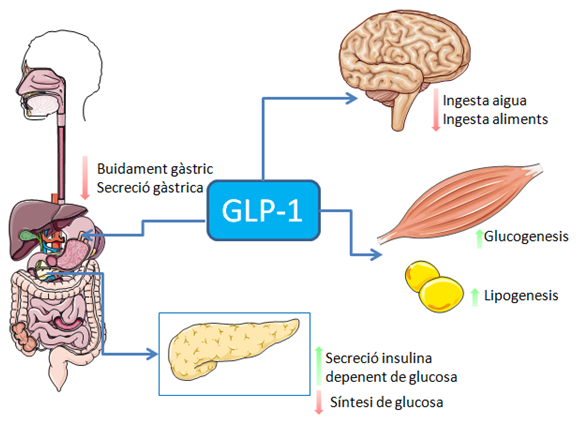
诺和诺德一直引领着 GLP-1(注,胃肠肽-1受体激动剂,用于治疗2型糖尿病和肥胖症药物)的开发,并且已经有一种口服 GLP-1上市。这种以 Rybelsus 为名的药物,只获得了美国食品药品管理局的批准,可用于治疗 2 型糖尿病,而不是肥胖症。
公司已经测试了一种治疗肥胖症的高剂量药片,并在 5 月份报告说,服用这种药片的患者在 68 周后体重减轻了 15.1%,而服用安慰剂的患者体重减轻了 2.4%。
High-Dose Semaglutide是semaglutide的改良口服制剂,与Rybelsus以及诺和诺德的注射剂Ozempic和Wegovy,使用的是同一种分子。
诺和诺德表示将在今年晚些时候,向美国食品药品管理局申请这种每日一次的大剂量减肥药的批准,这意味着可能在2024年获得批准。这将使诺和诺德领先任何潜在的口服 GLP-1 竞争对手数年,在抢占市场份额方面占得先机。
不过,还有一个重要的注意事项。目前还不清楚诺和诺德何时会真正选择将High-Dose Semaglutide药片投放市场,即使真的获得了美国食品及药物管理局的批准。因为诺和诺德在满足 Wegovy 的需求方面遇到了巨大困难。Wegovy 与大剂量减肥药使用相同的成分,推出新药可能会蚕食已经捉襟见肘的供应。
诺和诺德表示,High-Dose Semaglutide的上市取决于 “产品组合的优先次序和生产能力”。
TD Cowen分析师迈克尔·内德尔科维奇周一写道,这种药可能 “在一段时间内 “不会在肥胖症适应症领域上市。
礼来的Orforglipron
礼来公司是 GLP-1 领域的另一个巨人,正在开发一种名为Orforglipron的减肥药。上周末,公司表示在一项二期试验中,服用最高剂量 Orforglipron的肥胖或超重患者,在 36 周后体重减轻了 14.7%,而服用安慰剂的患者仅减轻了 2%。
高盛公司分析师克里斯·希布塔尼认为,这与诺和诺德公司的semaglutide药片和注射剂在类似时间内的表现相似。
与诺和诺德的High-Dose Semaglutide一样,礼来的Orforglipron也是每日服用一次的药片。与诺和诺德的药物不同的是,礼来的药物可以与食物同时服用,如果这两种药物在正面交锋中表现相似,这可能是一个优势。
礼来公司正在对orfoglipron进行一系列三期试验(注,药物开发过程中的关键阶段,评估药物的有效性、副作用等),这些试验必须在公司要求美国食品及药物管理局批准之前完成。公司预计时间最长的一项研究将于 2025 年年中完成,因此,Orforglipron有可能在 2026 年获得批准。
辉瑞公司的Danuglipron
辉瑞公司毫不掩饰争夺肥胖症和糖尿病市场的野心。这家制药巨头周一宣布了新药的选择:danuglipron,一种每日服用两次的药片。
公司放弃了另一种早期肥胖药lotiglipron,理由是在一些病人中发现肝酶水平较高,可能存在安全问题。辉瑞公司的股价大幅下跌,周一收盘时下跌了3.7%。关注的焦点似乎主要集中在Danuglipron每天需要服用两次,而礼来公司的Orfoglipron和其他药物每天只需服用一次。
花旗研究分析师丹尼尔·鲍姆预计Danuglipron将很难获得实质性份额。其他分析师则不太担心,高盛分析师写道,虽然选择Danuglipron 对辉瑞的影响 “趋势负面”,但抛售也过度了,辉瑞公司正在开发一种每日一次的Danuglipron,而且导致 lotiglipron 项目中止的安全性问题,在Danuglipron试验中没有出现。
辉瑞公司尚未公布计划中的Danuglipron三期试验的细节。如果试验于 2024 年开始,那么理论上说,如果一切按计划进行,药物可在 2027 年左右上市。
硕迪生物的GSBR-1290
硕迪生物的这种口服 GLP-1 药物,仍处于早期试验阶段。公司计划明年开始 2b 期试验。如果一切顺利,该产品将于 2029 年上市。投资者正在等待今年第四季度的 1b/2A 期数据。
硕迪生物股价周一大涨 18.4%,可能是由于辉瑞公司的声明令投资者感到失望,周二又下跌了 6.5%。
Terns制药公司的T-601
Terns制药公司是一家小型生物技术公司,正在开发一种名为 T-601 的口服 GLP-1 药物。最近几天,Terns的股价急剧下跌,自上周五收盘以来已下跌了 31%。部分原因可能与 Tern另一个针对肝脏疾病 NASH(注,一种肝脏疾病,与脂肪积累在肝脏内有关)的项目有关,但投资者似乎也受到了辉瑞消息的影响。T-601在结构上与Danuglipron 有一些相似之处,这似乎引起了人们对潜在肝脏问题的担忧。
瑞穗(Mizuho)分析师在周二写道:”我们预计肝酶升高不会成为 601 的一个问题,到目前为止,这还不是一个问题。
T-601是一个早期项目,上市时间尚不明确。


